問題29.多発性硬化症を合併した尋常性乾癬の患者に選択すべきではない薬剤はどれか.
1. IL-17 阻害剤
2. TNFα 阻害剤
3. IL-23 p19 阻害剤
4. エトレチナート
5. シクロスポリン
本問は、生物学的製剤の禁忌に関する出題です。
乾癬に対する生物学的製剤は、基本的に免疫を抑える方向に働きます。
そのため敗血症や結核などの「感染症」について禁忌なのは理解しやすいです。
ただ、「感染症」以外に禁忌があるのは不思議ですよね。
この記事では、「TNF-α阻害薬の添付文書上の禁忌」とそれぞれの「根拠」を解説しています。
第29問 TNFα阻害薬の禁忌【解答:2】

| 日本で承認のあるTNFα阻害薬 | 添付文書上の禁忌 |
| エタネルセプト (乾癬の保険適応なし) | ①敗血症の患者又はそのリスクを有する患者 ②重篤な感染症の患者 ③活動性結核の患者 ④本剤の成分に対し過敏症の既往歴のある患者 ⑤脱髄疾患(多発性硬化症等)及びその既往歴のある患者 ⑥うっ血性心不全の患者 |
| インフリキシマブ | ①重篤な感染症(敗血症等)の患者 ②活動性結核の患者 ③本剤の成分又はマウス由来の蛋白質 (マウス型、キメラ型、ヒト化抗体等) に対する過敏症の既往歴のある患者 ④脱髄疾患(多発性硬化症等)及びその既往歴のある患者 ⑤うっ血性心不全の患者 |
| アダリムマブ セルトリズマブ ペゴル ゴリムマブ(乾癬の保険適応なし) | ①重篤な感染症(敗血症等)の患者 ②活動性結核の患者 ③本剤の成分に対し過敏症の既往歴のある患者 ④脱髄疾患(多発性硬化症等)及びその既往歴のある患者 ⑤うっ血性心不全の患者 |
日本で承認されているTNFα阻害薬は、表の5種類です。(レナリドマイドもTNFα阻害作用がありますが今回は生物学的製剤に絞っています。)
添付文書上の禁忌は、文言に多少の違いがありますが、共通して以下の5つが挙げられます。
- 重篤な感染症(敗血症など)
- 活動性結核
- 同薬剤への過敏症の既往
- 脱髄性疾患(多発性硬化症など)とその既往
- うっ血性心不全
薬剤過敏症の既往については、薬剤一般にあてはまりますのでこの記事では触れません。
過敏症以外の4つについて禁忌の根拠について考えてみます。
重篤な感染症(敗血症)【有益なこともあるがごくわずか】
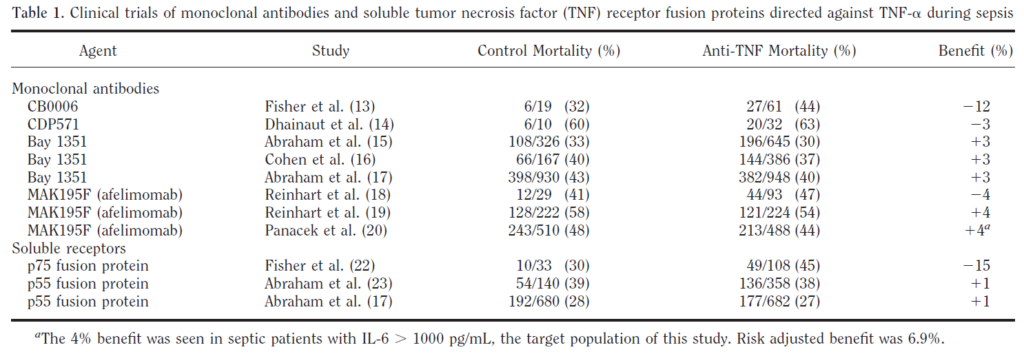
敗血症などの感染症は、「抗菌薬」と「補液・昇圧剤による全身管理」が治療の中心です。
一方、病原体に対する免疫反応による炎症も臓器障害につながります。
そこで「TNFα阻害による抗炎症がプラスに作用するのでは?」という敗血症に対するstudyが表のようにおこなわれました。
2001年の総説、2014年のメタアナリシス( Lv, S., et al. “Anti‐TNF‐α therapy for patients with sepsis: a systematic meta‐analysis.” International journal of clinical practice 68.4 (2014): 520-528. )によると、
- 敗血症の死亡率を必ずしも改善するわけではない。(良いという報告も悪いという報告もある)
- IL-6 > 1000 pg/mLのグループではわずかに有用かもしれない。
とされています。
このデータからすると、明確に禁忌にすべきかは微妙なところです。
ただ、敗血症に対して一貫して有用とは限らず、敗血症に対する適用承認も得られていないのが現状です。
免疫を抑える、という意味で禁忌になっていると考えられます。
活動性結核【インフリキシマブによる結核の有意な増加の報告】
| 関節リウマチ患者10万人あたりの1年の結核罹患率 | |
| インフリキシマブ未使用 | 6.2 |
| インフリキシマブ使用 | 52.2 |
結核に対するTNFα阻害薬が禁忌なのは、いまや常識となっていますが開発当初にはわかっていませんでした。
TNFα阻害薬使用後の結核発症はインフリキシマブで多く報告されています。
インフリキシマブ(レミケード®)は、1998年に米国FDAより「関節リウマチ」と「クローン病」に対する承認を取得しました。
その後、2001年にインフリキシマブ使用後に結核が発症したという報告(Keane, Joseph, et al. “Tuberculosis associated with infliximab, a tumor necrosis factor α–neutralizing agent.” New England Journal of Medicine 345.15 (2001): 1098-1104.)があり、
さらに2004年には表のように「インフリキシマブ使用中に結核罹患率が増加する」という報告が発表されています。
これらの報告を受けて、TNFα阻害薬使用時には「潜在性結核のスクリーニング」と「イソニアジド(INH)などの予防内服」が推奨されるようになりました。( Keane, J. “TNF-blocking agents and tuberculosis: new drugs illuminate an old topic.” Rheumatology 44.6 (2005): 714-720. )
スクリーニング・予防がない場合の「潜在性結核の再活性化」までの期間は、以下のように報告されています。
| 投与から潜在性結核の再活性化までの期間(中央値) | |
| インフリキシマブ | 12週間 |
| アダリムマブ | 4-6カ月 |
予防内服の期間については、ある総説(Cantini, Fabrizio, et al. “Guidance for the management of patients with latent tuberculosis infection requiring biologic therapy in rheumatology and dermatology clinical practice.” Autoimmunity reviews 14.6 (2015): 503-509.)によると、
- 潜在性結核の患者には、1-2カ月間予防内服後に生物学的製剤を使用すると活動性結核のリスクが下がる
- 活動性結核の場合には、少なくとも6カ月の治療後に生物学的製剤を再開するのがよいかもしれない
と記載されています。
以上をうけて、TNFα阻害薬では「活動性結核」が禁忌となっています。
脱髄性疾患(多発性硬化症など)とその既往【RCTで年間増悪頻度が増加】
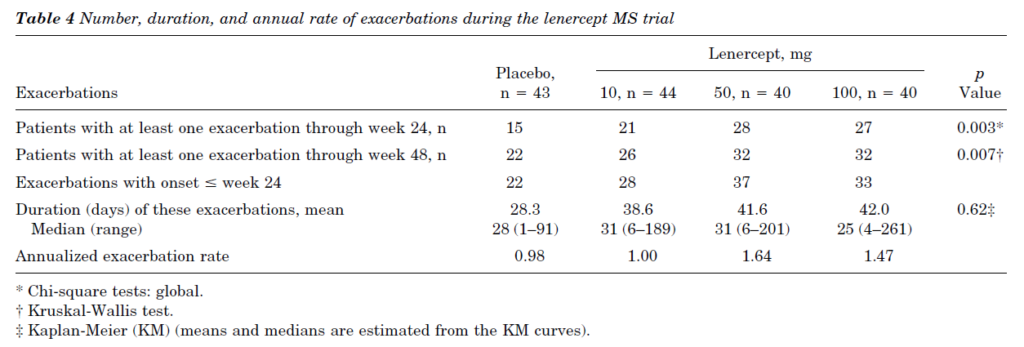
多発性硬化症での禁忌は、LenerceptのRCTにより確立されました。
Lenerceptはエタネルセプトと同様の構造を持つTNFα阻害薬です。
多発性硬化症の病変部にTNFの存在が報告されており、多発性硬化症に類似した「実験的自己免疫性脳脊髄炎(EAE)」を発症した動物に対するTNFα阻害が有効であったことから、Lenerceptについて多発性硬化症の第2相臨床試験としてRCTがおこなわれました。
しかしながら、結果はプラセボと比べて増悪頻度が増加(上表)しLenerceptが承認されることはありませんでした。
さらに、他のTNFα阻害薬使用中に多発性硬化症が発症する例も報告(Sicotte, Nancy L., and Rhonda R. Voskuhl. “Onset of multiple sclerosis associated with anti-TNF therapy.” Neurology 57.10 (2001): 1885-1888.)され、日本では禁忌になっています。
うっ血性心不全 【RCT(インフリキシマブ10ml/kg)で死亡・入院増加】
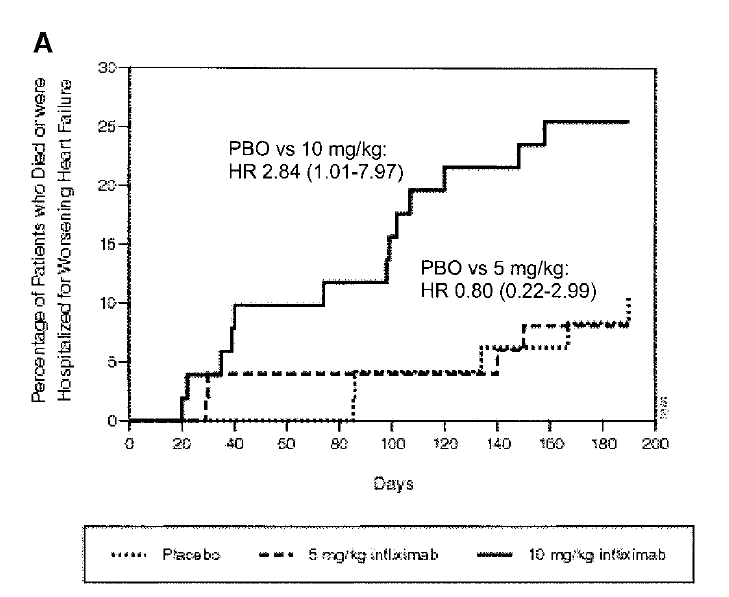
Figure 1より
うっ血性心不全での禁忌も、多発性硬化症と同様にRCTから確立されています。
心不全患者ではTNFαが上昇しTNFαは心不全の増悪につながるかもしれないという報告があり、NYHAⅢ-Ⅳの心不全患者に対してインフリキシマブを使用した第2相臨床試験としてRCTがおこなわれています。
結果は、図の通りで、5mg/kgの投与群ではプラセボと有意差がないものの、10mg/kgのインフリキシマブを投与した群では、投与開始28週以内の「死亡・入院率」がプラセボより有意に増加しました。
エタネルセプトでも同様のRCT(RECOVER試験・RENAISSANCE試験・RENEWAL試験)が組まれていましたが、有効性を示せませんでした。
これら結果を受けて日本の添付文書上「うっ血性心不全」でのTNFα阻害薬の使用は禁忌となっています。
まとめ【 過去の生物学的製剤の注意事項に関する出題 】

いかがでしたか?
TNFα阻害薬は、ほかの生物学的製剤と比べ禁忌が多いですが、過去の臨床試験の結果が反映されていたようですね。
TNFα阻害薬以外でも生物学的製剤に関する出題が過去問には散見されます。
生物学的製剤の注意事項に関する出題は、2019年度では第2問のIL-17阻害薬の副作用に関する出題につづけて本問は2問目です。
ほかの年度でも表のとおり出題があります。
| 出題内容 | |
| 2020年度第27問 | 生物学的製剤(デュピルマブ)と生ワクチン |
| 2018年度第17問 | IL-17A阻害薬3剤の共通点(添付文書) |
| 2017年度第20問 | IL-17A阻害薬3剤の投与スケジュール(用法用量) |
| 2014年度第14問 | 生物学的製剤(モノクローナル抗体)の命名法 |
| 2013年度第20問 | 乾癬に効果のある生物学的製剤 |
生物学的製剤の注意事項、特に添付文書からの出題が定期的にあります。
すべて暗記するのは難しいですが過去の出題分と関連する部分だけでも押さえておきたいところです。
参考文献

- エンブレル・レミケード・ヒュミラ・シムジア・シンポニー添付文書(2021年8月)
- Reinhart, Konrad, and Waheedullah Karzai. “Anti-tumor necrosis factor therapy in sepsis: update on clinical trials and lessons learned.” Critical care medicine 29.7 (2001): S121-S125.
- Lv, S., et al. “Anti‐TNF‐α therapy for patients with sepsis: a systematic meta‐analysis.” International journal of clinical practice 68.4 (2014): 520-528.
- Keane, J. “TNF-blocking agents and tuberculosis: new drugs illuminate an old topic.” Rheumatology 44.6 (2005): 714-720.
- Wolfe, Frederick, et al. “Tuberculosis infection in patients with rheumatoid arthritis and the effect of infliximab therapy.” Arthritis & Rheumatism: Official Journal of the American College of Rheumatology 50.2 (2004): 372-379.
- Cantini, Fabrizio, et al. “Guidance for the management of patients with latent tuberculosis infection requiring biologic therapy in rheumatology and dermatology clinical practice.” Autoimmunity reviews 14.6 (2015): 503-509.
- Lenercept Multiple Sclerosis Study Group and The University of British Columbia MS/MRI Analysis Group. “TNF neutralization in MS: results of a randomized, placebo-controlled multicenter study.” Neurology 53.3 (1999): 457-457.
- Sicotte, Nancy L., and Rhonda R. Voskuhl. “Onset of multiple sclerosis associated with anti-TNF therapy.” Neurology 57.10 (2001): 1885-1888.
- Chung, Eugene S., et al. “Randomized, double-blind, placebo-controlled, pilot trial of infliximab, a chimeric monoclonal antibody to tumor necrosis factor-α, in patients with moderate-to-severe heart failure: results of the anti-TNF Therapy Against Congestive Heart Failure (ATTACH) trial.” Circulation 107.25 (2003): 3133-3140.
最後に、こんな風に考えたら答えがかわるかもしれない、というご意見がありましたら、
ぜひコメント・ご意見いただけると嬉しいです。
←前問題 2019年度 第28問
アプレミラスト(オテズラ®)【エトレチナート・シクロスポリン・メトトレキサートと比較】
次問題 2019年度皮膚科専門医試験 第30問
第二世代抗ヒスタミン薬の投与可能時期
【禁忌、妊婦・授乳婦、肝腎機能障害、運転上の注意も解説】→



コメント